希少疾患「ドラッグロス」拡大 欧米ベンチャーと連携不足
米国で実用化された希少疾患の新薬が、日本では臨床試験などの承認申請に向けた開発すらされていない「ドラッグロス」と呼ばれるケースが急増しているとの分析結果を、名古屋市立大などのチームがまとめた。新薬開発の担い手として欧米で存在感を増すベンチャー企業と、日本企業との連携が不十分なのが要因と指摘した。
名古屋市立大の児玉耕太教授は「開発の早い段階から外資系のベンチャーに日本企業がしっかり投資、連携できるよう後押しをする必要がある。国内のベンチャーを育成する取り組みも重要だ」と話す。
希少疾患は約7千種あるとされるが、約95%が有効な薬がない。患者数が少なく、開発コストがかかる一方で、収益性が低いなどとされ、創薬の主体はベンチャーや研究機関となりつつある。
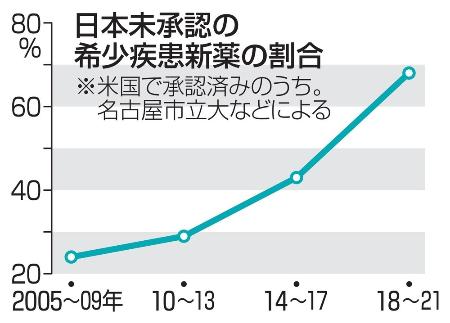
チームは、2005~21年に米国で承認された希少疾患薬249製品を分析。うち日本未承認なのは120製品、開発すらされていなかったのは86製品だった。
米国で承認された希少疾患新薬で日本未承認のものの割合は増え続けており、18~21年では68%に達した。この間、米国で承認された新薬の半分以上はベンチャー発。外資系ベンチャーのうち、自力で日本での開発をしたのは27%だった。
ベンチャー発の製品の多くは、米国での開発が最終段階に入ってから日本企業や日本に拠点のある外資系企業と連携し始める傾向にあり、日本での承認が遅れる要因となっている可能性がある。
成果は国際専門誌「ドラッグ・ディスカバリー・トゥデー」に掲載された。
医療・健康の記事一覧
-
社説(4月27日)機能性表示食品 制度検証し安全確保を


-
RSウイルス「流行入り」 静岡県が注意呼び掛け


-
整骨院療養費 6月から0.26%上げ 初検料30円増


-
全国コロナ感染 11週連続で減少


-
マダニ媒介感染症 静岡県内で今年2例目

-
健康被害の疑い 静岡県内新たに5人 紅こうじ問題

-
iPS心筋移植でサルの梗塞改善 慶応大、不整脈抑える

-
エステーに再発防止命令 「花粉を香りでガード」根拠なし

-
健康被害、半数に基礎疾患 大阪市、紅こうじ症例解析

-
小林製薬、外部有識者会議を設置 「紅こうじ」の対応検証

-
富山の製薬会社に業務停止命令 虚偽の試験結果を作成

-
コロナ感染、11週連続減少 前週比0・98倍

-
人工ぼうこう、肛門造設 オストメイトに理解を 静岡県内で入浴・プール利用拒否相次ぐ

-
小学1校 学級閉鎖 静岡県内インフルエンザ

-
健康被害の疑い 静岡県内新たに1人 紅こうじ問題

-
ALS治療薬の研究成果を解説 5月12日、浜松市で特別講演会

-
健康食品の広告、73%が不適切 臨床試験の都合良い結果強調

-
金融所得で保険料増を検討 医療介護、不公平見直し 事務負担に課題、自民PT

-
万博の「人工心臓」パソナ公開 開発者「移植に代わる夢」

-
医療逼迫時、緊急宣言も 感染症対策 政府計画改定案 柔軟に切り替え

-
米で患者にブタの腎臓移植 2例目、遺伝子改変少なく

-
関節手術支援ロボ導入 静岡県内初の聖隷三方原病院、安全性向上と術後入院短縮へ

-
後発薬、業界再編求める報告書案 安定供給へ集中改革期間

-
AIで胃がん進行度合い判断 高精度達成、年内実用化へ

-
頸動脈の塊から微小プラ 脳卒中4倍、伊の研究チーム発表

-
感染症の行動計画案を了承 医療逼迫時に緊急事態宣言

-
大自在(4月24日)熱中症特別警戒アラート

-
記者コラム「清流」 はしかの恐ろしさ

-
1小学校学級閉鎖 静岡県内インフルエンザ

-
新型手術支援ロボット用いて成功 助手2人分1台で、名市大病院

-
マイナ不可「通報」文書問題なし 河野氏、保険証利用巡り

-
患者と医師「女性同士」が有益 東京大など調査、死亡率など低く

-
マダニ媒介感染症 静岡県内で今年初確認 中部60代女性

-
健康被害の疑い 静岡県内新たに2人 紅こうじ問題

-
生きがいづくり活動支援、推進員8人委嘱 しずおか健康長寿財団

-
帯状疱疹ワクチン一部助成 御殿場市、50歳以上対象

-
ドライアイの改善

-
ステロイド外用剤 塗り方や部位に注意【もっと広がる クスリの世界】

-
短鎖脂肪酸で持久力向上【未来は腸内細菌とともに⑬】

-
その動悸や息切れ、本当に更年期障害? 「心房細動」女性も注意 閉経境に急速に増加

-
気候変動、労働者7割に健康被害 ILO推計、保護の必要性指摘

-
ヒルドイド、10月に自己負担増 保湿薬、医療費抑制で厚労省

-
働くがん遺伝子 画像解析 個別化医療に期待

-
生え替わり時期 歯磨きしっかり

-
「紅こうじ」静岡県内健康被害50人に 新たに2人確認 小林製薬サプリ

-
全国コロナ感染 10週連続で減少

-
静岡県内インフル患者、前週から半減 4月8~14日、コロナも減

-
小林製薬紅こうじサプリ原料 未想定物質さらに複数 国の分析で検出

-
がん教育を大人にも/ワクチン接種推奨 静岡市が対策計画見直し

-
0歳男児、ジェット機で搬送 1例目、石川から愛知へ

-
エムポックスに新派生型か コンゴ、人から人への拡大懸念

-
コロナ感染者、10週連続減少 1医療機関当たり3・71人

-
厚労相、地域別診療報酬に慎重 医師不足なら患者負担高く

-
機能性食品の在り方を初議論 信頼性確保へ改善点探る

-
日本に新たな国際保健拠点 WHO、世銀と25年設置

-
静岡県内3施設で学級閉鎖 インフルエンザ

-
小林製薬「紅こうじ」健康被害疑い 静岡県内で新たに1人 患者48人に

-
聖隷浜松病院に消化器センター 小児から成人へ移行期医療、適切に

-
紅こうじサプリ健康被害、静岡県内で新たに2人 計47人に

-
4施設で学級、学年閉鎖 静岡県内インフルエンザ

-
「あすはわが身」 謙虚に【アラ還 2人の がん奮闘記⑨】

-
日本医師会、地域別報酬に反対 偏在対策「筋の悪い提案」

-
「紅こうじ」健康被害、新たに2人 静岡県内患者は計45人

-
受動喫煙肺がん 「変異」で悪化か 特有の遺伝子型 喫煙者には確認できず

-
4施設学級閉鎖 静岡県内インフルエンザ

-
医師偏在是正へ地域別報酬 財務省、薬剤費抑制も提言

-
重大感染症 行動計画10年ぶり抜本改定 流行初期でも緊急事態宣言

-
感染症流行初期でも緊急事態宣言 行動計画、10年ぶり抜本改定

-
受動喫煙肺がん特有の遺伝子変異 たばこを吸う人とは異なる型

-
医師の偏在是正へ地域別報酬 財務省審議会、薬剤費抑制も提言

-
浜松の小学校で学級閉鎖 静岡県内インフルエンザ

-
健康増進テーマに女性向けセミナー 静岡厚生病院で5月18日に

-
「健康づくりサポーター」日本旅行静岡支店に登録証 いきいきフォーラム21

-
膵臓がん 検査キット登場 早期のダメージ捉える 検診への応用にも期待

-
話題の成分「短鎖脂肪酸」【未来は腸内細菌とともに⑫】

-
矯正で歯肉下がった 移植手術で改善も【歯の診察室】

-
コロナワクチン心筋炎注意 厚労省、子どもで2例報告

-
脊髄難病の胎児手術成功、阪大 母親の子宮切開で日本初

-
高齢者、運転中止前に代替検討を ドライバー増加で老年学会提言

-
薬標的の遺伝子変異15% 日本人の検査データ5万件分析

-
子どもの「片頭痛」 大人と違う症状、薬が効かないタイプも

-
愛知で6歳未満男児が脳死 心臓を移植

-
インフル患者半減、注意報レベル下回る 静岡県内、コロナも減 4月1~7日

-
静岡県内2校 学級閉鎖 インフルエンザ

-
全国コロナ感染 9週連続で減少

-
心血管疾患で配偶者うつリスク増 発病した世帯を調査

-
静岡の介護施設で食中毒 18人が下痢症状訴え

-
コロナ感染者数、9週連続減 1医療機関当たり4・26人

-
付き添い入院、病院が要請44% こども庁が実態調査

-
中学1校 学級閉鎖 静岡県内インフルエンザ

-
肺がん疑い見逃し、80代死亡 名古屋大病院、遺族に謝罪

-
「紅こうじ」健康被害、静岡県内新たに4人 患者は計39人に

-
富士市、新興感染症に備えコロナ対応録公開

-
静岡県の感染症対策 センター長が解説 13日、富士で講演会

-
ウイッグ探しに苦労【アラ還 2人の がん奮闘記⑧】

-
米が飲み水のPFAS濃度基準を決定 世界的にも厳しい水準

-
紅こうじ論文は「適正」と著者 販売後の品質確認が重要と指摘

-
医療城下町を発展、住民に成果還元へ 静岡県東部「ファルマバレー」 新局面へ手探り続く

-
紅こうじサプリ 青カビ混入なら「異変気付くのでは」 有識者が指摘

-
遺体の歯科記録照合、技術学ぶ 災害時などに備え医師会研修会 静岡市駿河区

-
25年4月に感染症の新機構設置 次のパンデミック備え

-
死亡5人中3人に既往歴 70代3人、紅こうじサプリ

-
マイナ保険証利用率5・47% 促進へ病院に最大20万円支給

-
紅こうじ健康被害疑い 静岡県内で新たに6人

-
自宅で「加熱式」 改正法施行4年 受動喫煙懸念 家庭内、近隣にも被害

-
微生物からの贈り物【未来は腸内細菌とともに⑪】

-
機能性表示食品 果物、魚など生鮮食品も【知って、いかす 健康食品③】

-
医師の情報共有アプリ提供 キヤノン系、働き方改革へ

-
感染症対策拠点が本格始動 三島、旧県総合健康センター改修

-
GID(性同一性障害)学会が「日本GI(性別不合)学会」に 「障害ではない」意識拡大

-
23人新たな学び 静岡社会健康医学大学院大で入学式

-
医療ケア児支援へ 浜松市中央区に相談拠点

-
紅こうじ「原因解明を」 サプリ2年常飲、腎機能低下の男性

-
「はしか」高まる警戒感 子どもの定期接種を確実に 静岡県、冷静対応呼びかけ

-
急患対応拡充へ一歩 富士市立中央病院 救急専門医を初配置

-
紅こうじ健康被害疑い 静岡県内で新たに2人 公表遅れ、国の指針に抵触か

-
浜松医科大で入学式 「信頼される医療人に」

-
静岡看護専門学校で入学式 看護師の道へ一歩 静岡市駿河区

-
水道水に基準超え有害物質 秋田、職員が加水し隠蔽

-
「必要なルールを検討」厚労相 紅こうじ健康被害

-
「非倫理的で危険」と学会声明 子どもへの頭部磁気治療で

-
バイオ3Dプリンターで神経再生 26年にも実用化、京都大

-
ブタ腎臓移植の男性退院、米国 透析治療からの離脱に「感激」

-
伊東の旅館利用者で4人食中毒 ノロウイルスを検出

-
コロナ後遺症 半数以上に 21年以前の感染で7割 静岡県追跡調査

-
【紅こうじ問題】静岡県内の健康被害 新たに1人確認

-
シャワーだけで毛が抜ける【アラ還2人のがん奮闘記⑦】

-
歓迎会一気飲み「NO」呼びかけ コロナ5類後初のシーズン

-
【時評】麻疹対策のワクチン 抗体獲得へ2回接種を(矢野邦夫/浜松医療センター感染症管理特別顧問兼浜松市感染症対策調整監)

-
「人食いバクテリア」劇症型溶連菌 全国の患者 最多ペース

-
iPS心筋シート移植の治験へ 阪大、拡張型心筋症の重症化防げ

-
「劇症溶連菌」患者、最多ペース 昨年上回る、毒素多い株も

-
高温多湿で雑菌発生のリスク 紅こうじ、細心の注意が必要

-
【紅こうじ問題】静岡県内の被害患者、新たに7人確認

-
オプジーボ効果を予測 京大など成功 がん患者の血液から

-
御殿場のこども園 インフルエンザで学年閉鎖

-
コーヒーが認知症リスクに影響

-
突然死呼ぶ 大動脈瘤破裂 自覚症状なく 早期発見で予防治療

-
自分に合う菌種探して【未来は腸内細菌とともに⑩】

-
接種後に不安大幅解消 子宮頸がんワクチン、岡山大調査

-
米で鳥インフルエンザ、人に感染 高病原性2例目、牛と接触

-
オプジーボ、血液で効き目を予測 がん患者治療、効率的に

-
「オーラルフレイル」にご用心 口の機能低下、全身に影響

-
医療ジェット試験運航開始、愛知 NPO法人、小児患者救命目指す

-
75歳以上保険料、月7082円 24年度平均、507円増

-
コロナワクチン順次廃棄、厚労省 1500万回分以上

-
微生物の働き 有機物を分解、有用な物に(細矢剛/国立科学博物館植物研究部長)【発酵のひみつ①】

-
紅こうじ健康被害相談 静岡県など31都府県で確認

-
伊東の歯科保健専門員 竹安さんに功労者表彰 園児、児童ら対象「はみがき教室」継続

-
分娩病院半数で「宿日直許可」 休息とみなし労働時間とせず

-
50代男性脳死判定 静岡県内病院に入院

-
感染症対応 ドクターカー 静岡県立こども病院が導入

-
静岡がんセンター病棟にオンライン学習室 若者世代交流の場に 元患者の女性、改修費全額寄付

-
【紅こうじ問題】静岡県内の健康被害計9人に 県と静岡、浜松両市が電話相談窓口設置

-
静岡県内インフル、新型コロナともに前週比減

-
紅こうじサプリ 静岡県内疑い患者計6人 県「直ちに摂取やめて」

-
孤独感「ある」が39%、横ばい 23年政府の2万人調査

-
【紅こうじ問題】富士市立中央病院で腎疾患入院2件 原因はサプリ濃厚

-
PETがん検診 受診券販売開始 4月1日から、遠鉄百貨店

-
医科大学院大の計画検討委 委員長に京大副学長 静岡県

-
急拡大の市場に暗い影 小林製薬の紅こうじ問題 機能性食品、広がる不安【表層深層】

-
伊豆の温泉活用 新産業を提案 沼津で成果発表会

-
マカダミアナッツを追加 アレルギー表示見直し

-
経鼻インフルワクチン申請 スプレー式、阪大微研

-
「認知症との共生社会に」初会合 当事者参加、秋に基本計画決定へ

-
育児中ストレス、腸内環境と関連 母親調査、京大

-
紅こうじ商品摂取 浜松市保健所に相談「腎機能の数値悪化」 静岡県が国に報告

-
シャンソン化粧品(静岡市) 紅こうじ使用の健康食品回収 被害確認されず

-
疲労困憊の点滴治療初日【アラ還 2人の がん奮闘記⑥】

-
中卒者、死亡率1・4倍 がん検診の低迷、喫煙が影響か

-
ウーバー、全国で処方薬を配達へ 薬局チェーンなど4社と提携

-
希望者が臓器移植できる社会を 患者団体ら、厚労省に要望

-
高齢者保険料、4月から引き上げ 医療、75歳以上540万人対象

-
心臓移植の女児が支援に感謝 募金5億円超を引き継ぎ、川崎

-
静岡県内被害確認されず 小林製薬の紅こうじ問題

-
補助金211億円を不正申請 東京、コロナ検査で17事業者

-
難病「遠位型ミオパチー」薬承認 世界初、筋力低下の進行抑える

-
1型糖尿病に「20歳の壁」 助成途切れ 望む治療諦める患者も 専門医 公的支援訴え

-
災害時に備えて 服用情報 常に把握を【もっと広がる クスリの世界】

-
腸内フローラの好物は?【未来は腸内細菌とともに⑨】

-
厚労相「役割重要だった」と感謝 コロナ専門家組織廃止で

-
どうなる?2024年問題 物流/バス・タクシー/建設業/勤務医【Q&Aまとめ】

-
認知症ソフトボール、富士宮で全国大会 工藤公康さん視察、声援送る

-
薬の不足状況、随時公表へ 厚労省HPで、4月から

-
医療知識「社会に還元、貢献を」 静岡社会健康医学大学院大

-
30年ぶり肥満症の新薬販売 ウゴービ、食欲抑制作用

-
外国人材の訪問介護、拡大へ 特定技能解禁、24年度にも

-
世界初、ブタの腎臓を患者に移植 米病院、臓器不足緩和へ

-
インフル「注意報」再発令後も拡大 静岡県内、コロナも前週比増

-
婚姻・妊娠届提出で葉酸サプリ配布 三島市、4月1日から

-
帯状疱疹ワクチン 5月から接種助成 三島市

-
がん患者が減少、コロナ影響か 20年、登録94万5055人

-
新型コロナ感染者、6週連続減少 3万316人、前週比0・94倍

-
静岡県が基準病床設定 全8医療圏「過剰」

-
世界平均寿命1・6歳短く 新型コロナ流行2年間

-
ステージ4の衝撃【アラ還 2人の がん奮闘記⑤】

-
エクソソーム使用、指針策定へ 再生医療学会、4月にも

-
静岡県内2施設で学級閉鎖 インフルエンザ

-
野菜摂取状況を推定 官民連携でイベント 静岡市葵区

-
地域医療見直し、議論開始へ 高齢者ピークの2040年見据え

-
国内はしか発症相次ぐ 同じ航空機の帰国者ら

-
患者、医師双方の時間短縮 大阪・河内長野市が遠隔診療実験

-
インフルエンザ 静岡県内4施設閉鎖

-
介護報酬のコロナ特例廃止 接種の送迎、4月から

-
むし歯のできやすさは遺伝? むし歯菌や食べ物も原因【歯の診察室】

-
生活スタイルが決め手【未来は腸内細菌とともに⑧】

-
60代男性脳死判定 静岡県内病院

-
発達障害は診断名ではない 「言葉が独り歩き、親たち不安に」 小児科医/成田奈緒子さん

-
生体・生活データで認知症選別 大分大など 有害タンパク質の蓄積予測

-
症状入力で「希少疾患」情報検索 京大やIBMの研究チーム

-
PFAS 夏に除去指針 環境省、健康への影響懸念

-
【科学する人】「毒」にするスイッチ発見 がん光免疫療法を開発 小林久隆さん㊥

-
緩和ケア病棟が完成 藤枝市立総合病院 静岡県中部で唯一

-
糖尿病予防調査、大学院大と連携 静岡市が協定締結

-
静岡県内8施設で学級、学年閉鎖 インフルエンザ

-
医師試験9547人合格 厚労省発表

-
コロナ専門家組織、3月末廃止へ 20年2月から124回開催

-
コロナ定期接種、7000円に 24年度、65歳以上高齢者ら

-
23施設で学級、学年閉鎖閉鎖 インフルエンザ

-
男性接種、費用対効果に課題 HPVワクチンの定期化議論

-
5歳未満死亡数490万人 ユニセフ報告書 支援向上、過去最少

-
静岡県、コロナ病床確保終了へ 注意報、警報の発令制度は継続

-
新型コロナ電話相談窓口、3月末終了 静岡県と静岡、浜松両市

-
手術直後の負担 予想外(藍田紗らら/ライター)【アラ還2人のがん奮闘記④】

-
静岡県内39施設で学級、学年閉鎖 インフルエンザ

-
浜松医大卒業式、225人巣立ち 「命の尊さを感じ、今後も日々学び精進」

-
コロナ脳症重くなりやすく 死亡・後遺症が25%超

-
コロナ後遺症に経済支援を 患者ら、署名呼びかけ

-
救急搬送時、マイナ保険証を活用 受診歴取得、67消防で実証

-
静岡県内23施設で学級、学年閉鎖 インフルエンザ

-
慢性疲労症候群の臨床試験へ 今夏、抗体薬「リツキシマブ」

-
手術ミス、2600万円賠償 香川県立中央病院が遺族に

-
致死量の薬の投与認める法案発表 仏で5月から審議、終末期患者に

-
フローラ 外からの影響反映【未来は腸内細菌とともに⑦】

-
殿様枕症候群にご注意 高すぎると脳梗塞リスク 首の動脈の病気と関連か

-
人工甘味料 ダイエットには勧められない【知って、いかす 健康食品②】

-
静岡県内13施設で学級、学年閉鎖 インフルエンザ

-
食中毒発生、2年連続増 23年、コロナ禍前の水準に

-
ドナネマブ、米承認さらに遅れ リリーのアルツハイマー薬

-
勤務医の残業規制、9割守れず 特定機能病院、4月の働き方改革

-
独男性、コロナワクチン217回 60代が接種か、異常確認されず

-
発災直後の情報整理重要 浜松赤十字病院DMAT報告 能登地震

-
新型コロナ「注意報」解除 静岡県、医療レベルも「通常」に引き下げ

-
静岡県内10校で学級、学年閉鎖 インフルエンザ

-
認知症の情報交換 カフェで気軽に 清水町で当事者ら

-
心疾患の高リスク見逃し大幅減 新潟大、メタボ診断基準に修正案

-
新型コロナ感染、4週連続で減少 1医療機関当たり6・99人

-
医療的ケア児、体制整備に遅れ 文科省へ改善要請、家族離職防止

-
はしか、厚労相が注意喚起 関空到着便の5人感染確認

-
静岡県内10小学校で学級閉鎖 インフルエンザ

-
島根大、心疾患で世界初手術成功 別難病も同時改善

-
静岡県内31施設で学級、学年閉鎖 インフルエンザ

-
医療体制や最新技術学ぶ 開発途上国行政官 静岡県立総合病院でJICA研修

-
オウム病、欧州で5人死亡 WHO、昨年11月以降

-
コロナ公費支援 3月末終了 薬 負担増、入院補助廃止

-
静岡県内17施設で学級、学年閉鎖 インフルエンザ

-
医療、福祉、司法 専門職が相談会 9日、静岡と伊豆

-
ゾコーバ、改めて承認取得 塩野義、患者同意書不要に

-
コロナ公費支援、月末で終了 4月から薬代負担増、厚労省通知

-
医療従事者、うつ症状36% 人員不足と多忙、自治労

-
コロナ公費支援、3月末で終了 薬代負担増、入院補助も廃止

-
静岡県内6施設で学級閉鎖 インフルエンザ

-
睡眠薬の使用やめたい まずは別の種類に変更を【診察室】

-
低用量ピルをオンラインで 生理の症状 通院せず軽減 処方サービス広がる

-
コロナ薬ゾコーバ、改めて承認へ ダニ媒介脳炎ワクチンも

-
京大、肺と肝臓を同時に生体移植 世界初、男児に両親と祖父が提供

-
大正製薬、内蔵脂肪の減少薬発売 食べた25%を便とともに排出

-
マラリア撲滅へタッグ継続 塩野義と長崎大、5年間

-
忙しくても朝食を(保井智香子/立命館大教授)【カンタンおいしい 健康レシピ⑩】

-
やせすぎ「不調の原因に」 適正体重の大切さ伝える

-
「下戸」の日本人、2段階で増加 2万年前&7500年前 1万人ゲノム解析 国立国際医療研など

-
空飛ぶドクターカーを試験飛行 宮崎、27年度実用化目指し

-
高齢者のがん医療説明 長泉、5年ぶり対面「会議」

-
浜松医大、中学生が取材 医療現場を理解 「記事」執筆へ

-
【科学する人】精子バンクの再開目指す 男性の不妊治療に取り組む 岡田弘さん㊦

-
はしか、欧州急増し世界的に流行 ワクチン接種減影響か、日本でも

-
米、コロナで5日間の隔離撤廃 症状改善すれば復帰可能に

-
静岡県内「インフルエンザ警報」解除 新型コロナは注意報継続

-
静岡県内4施設で学級閉鎖 インフルエンザ

-
PTSD引き起こす分子機構解明 東大チーム、世界初

-
「第10波」ピーク越えた可能性 コロナ、感染者3週連続減

-
静岡県内9施設 学級、学年閉鎖 インフルエンザ

-
難病・遠位型ミオパチー薬承認へ 世界初、筋力低下の進行抑制期待

-
治療標的の遺伝子変異15% がん種ごとに大きな差

-
救急安心電話相談「#7119」 効果検証へ協議会 静岡県議会、川勝知事表明 2025年度本格運用目標

-
看護・介護体験談を募集 オレンジクロス(東京都)

-
手術時連絡先 やっと提出(藍田紗らら/ライター)【アラ還 2人のがん奮闘記②】

-
更年期障害、7割が自覚症状

-
認知症新薬の治療開始 浜松・聖隷三方原病院 女性2人に点滴投与 静岡県内4施設目

-
静岡県内10施設で閉鎖 インフルエンザ

-
静岡県内7施設で学級閉鎖 インフルエンザ

-
病気との関係 明らかに【未来は腸内細菌とともに⑤】

-
不潔への不安 過剰な確認 強迫性障害 見過ごすと重症化の恐れ

-
グレープフルーツに注意 薬を分解する働き阻害【もっと広がる クスリの世界】

-
コロナ感染者、2週連続減 1医療機関当たり10・10人

-
インフル患者数、1カ月半ぶり減 B型最多、前週比0・86倍

-
人工臓器で受精卵着床再現 細胞の融合観察、東北大

-
独、大麻合法化の法案可決 医師ら根強い反対

-
小学生のほぼ半数が花粉症を実感 ロート製薬の調査、生活に影響も

-
静岡県内 新型コロナ警報解除、注意報に インフルは継続

-
静岡県内16施設で閉鎖 インフルエンザ

-
静岡県内16施設で閉鎖 インフルエンザ

-
災害歯科の「調整役必要」 静岡県歯科医師会 体制確立へ、駿河区で研修会

-
「おひとり様」の助け合い(藍田紗らら/ライター)【アラ還 2人のがん奮闘記①】

-
介護職労組が賃上げ要求 人手不足で「ケアに影響」

-
新出生前診断で新ルール 対象拡大時は学会が意見

-
体内で遺伝子改変も対象に 再生医療法の改正案、提出へ

-
マラリアの高精度検査法を開発 愛媛大、ガーナで研究開始

-
静岡県内14施設 インフルエンザで学級、学年閉鎖

-
新型コロナ 公費支援 3月で終了 来年度から通常医療移行

-
奥能登、看護師離職相次ぐ 拠点4病院、自宅被災も

-
新型コロナ、公費支援3月で終了 24年度から通常医療体制に移行

-
患者3人死亡、徳洲会に改善命令 神戸市、安全管理体制に不備と

-
情報豊富な「茶色い宝石」【未来は腸内細菌とともに④)】

-
立ったままCT 機能の衰え発見後押し 慶応大と民間企業開発

-
飲酒少量でも高血圧リスク 健康に配慮留意点も 厚労省初の指針 「純アルコール量に着目 重要」

-
病院薬剤師確保へ 静岡県が就職説明会 23日、全国の薬学生対象

-
静岡県に医科大学院大設置へ提言 横断的な研究推進など明記 準備委

-
4歳児、言葉が舌足らず 舌の大きさ、歯並びが影響【歯の診察室】

-
歯周病予防テーマ 25日に講演会 静岡県立中央図書館

-
透析中の症状5カ国語に 順大保健看護学部生が「日本語対比表」作成 外国人と医療者の不安解消

-
飲酒、少量でも高血圧リスク 健康に配慮、厚労省が初の指針

-
運動時はスポーツ飲料【カンタンおいしい 健康レシピ⑧】

-
若手の定着目指しベテラン医師指導 静岡県立総合病院

-
肝疾患予防法 医師らが講話 裾野で24日

-
トカゲは人よりグルメ? 近大など 味覚遺伝子特定

-
【科学する人】男性の不妊治療に取り組む 岡田弘さん㊤ 精子採取、多くの症例

-
盲導犬歩行、VRを開発 東大チーム 多様な視覚障害の理解促進

-
背骨の曲がり放置しないで 思春期特発性側彎症 装具で進行抑止

-
清水病院へ9億円補てん 静岡市24年度予算案

-
新型コロナ、インフルともに患者数減 静岡県、警報は継続

-
静岡県内25施設で学年、学級閉鎖 インフルエンザ

-
コロナ感染者、3カ月ぶり減 石川が全国最多、次いで愛知

-
静岡県内34施設で学級・学年閉鎖 インフルエンザ

-
経口中絶薬「郵送使用も安全」 米研究、制限の動きけん制

-
被災地ボランティアに無料接種 破傷風ワクチン、東京の医師団体

-
インフルで静岡県内27施設学級・学年閉鎖 浜松の2校は学校閉鎖

-
コロナ感染で慢性疲労リスク4倍 米、後遺症頻度高く「予防策を」

-
初診料、最大730円増 賃上げ原資、24年度報酬改定

-
静岡県内8施設で学級閉鎖 インフルエンザ

-
国内初、人に移植できるブタ誕生 遺伝子改変で拒絶反応回避

-
成長期 鉄不足で貧血【カンタンおいしい 健康レシピ⑦】

-
医療的ケア児、災害時に支援を 大阪で保護者らイベント

-
マーモセット実験活用拡大 新潟大と富山大チーム 異種間の卵巣移植

-
望む終末期の医療 家族と話し合って 浜松市天竜区で講演会

-
免疫抑制剤の不使用2%未満 肝移植後、欧米より少なく

-
新生児希少疾患検査 静岡県内35施設で導入へ 「発症前の確知」が鍵、普及目指す

-
静岡県、W警報のインフルとコロナ ともに患者が前週比増

-
静岡県内の小中学校13施設で学級・学年閉鎖 インフルエンザ

-
44道府県、感染症備え 3万3000床確保 厚労省、上積み目指す

-
全国 コロナ 「第10波」に 11週連続増

-
原薬の不適切製造で業務改善命令 富山県、アクティブファーマに

-
受精卵作製、研究対象を拡大 政府、遺伝病や核移植の指針改正

-
「ショック大きい」 地域住民から不安の声 引佐赤十字病院閉院へ

-
新型コロナ「第10波」に 11週連続増、石川が最多

-
インフル患者が4週連続増 警報級8府県、福岡最多

-
コロナ禍「死にたい」増加 20歳未満外来患者が1・6倍に

-
浜松・引佐赤十字病院 2025年3月末閉院 施設老朽化、患者減

-
静岡県内22施設で学級・学年閉鎖 インフルエンザ

-
透析の医療費助成 浜松市に継続要望 静岡県腎友会

-
胎盤模した人工臓器を作製 医薬品開発へ活用期待

-
コロナ治療薬、公費支援継続を 4月以降も、3学会が要望

-
静岡県内42施設で学級・学年閉鎖 インフルエンザ

-
冬場のお風呂の入り方 ヒートショックに気をつけて【高齢者の相談室】

-
静岡県内29施設で学級・学年閉鎖 インフルエンザ

-
日本脳炎、接種漏れに注意 不足解消も最大200万人

-
胎児にブタ腎臓を一時移植計画 慈恵医大、実現なら国内初事例

-
マイナ保険証、公務員利用も低迷 推進側が4%、厚労相危機感示す

-
静岡県内20施設で学級・学年閉鎖 インフルエンザ

-
精神科診療、対面と比較 オンラインでも同等の効果

-
米CDC、東京に事務所 感染症流行に備え

-
匿名提供巡り当事者が対談 生殖補助医療で

-
オーバードーズ疑い搬送5千人 23年上半期、若年層目立つ

-
新型コロナ警報発令 静岡県、インフルと同時流行 ダブル警報は初

-
ネイルチップで闘病中も前向きに 浜松のサロン、展示見本を再利用

-
がん治療と仕事の両立 休職制度や在宅勤務利用【ライブセミナー】

-
温泉と医療が連携 宿泊プラン提案も 静岡県、下田でフォーラム

-
静岡県内25施設で学級・学年閉鎖 インフルエンザ

-
インフルエンザ3週連続増 福岡と沖縄で警報レベル

-
コロナ感染者、10週連続で増加 前週比1・22倍、厚労省

-
花粉避け、早めに薬を シーズン前に予防呼びかけ

-
「よくかんで食べる」テーマに総菜パン 杏林堂と聖隷福祉事業団が健康課題解決へ

-
静岡県内20施設 インフルエンザで学級、学年閉鎖

-
「フレイル」予防へ講演 シニア世代100人参加 静岡市駿河区

-
新規がん患者、世界で2千万人 22年推計、治療格差に警鐘

-
米製薬企業、認知症薬の販売終了 アデュカヌマブ、高額で普及せず

-
静岡県内41施設で学級、学年閉鎖 インフルエンザ

-
空間除菌で優良誤認表示 消費者庁、4社に措置命令

-
マイナ保険証で医療費10割請求 23年10月以降753件

-
中国、鳥インフル感染の女性死亡 春節大移動で拡大警戒

-
不妊治療の負担軽減へ 静岡県が先進医療費助成 43歳未満、1回当たり5万円上限 24年度予算案

-
静岡県内32施設で学級・学年閉鎖 インフルエンザ

-
山梨県が卵子凍結助成へ 将来妊娠や出産望む女性に

-
マスク氏企業、脳にチップ初移植 手足まひ患者に臨床試験実施

-
訪問看護、要件見直しへ 精神科の不正請求で厚労相

-
周産期心筋症 発見早期に 妊娠、出産期に心機能低下 兆候の息切れ 注意

-
静岡県内15施設で学年・学級閉鎖 インフルエンザ

-
札幌で6歳未満男児が脳死 心臓、肝臓、腎臓を移植

-
救急車到着、初の10分超 22年、出動件数も過去最多

-
救急相談は電話で「#7119」へ 静岡県、10月にも導入方針

-
劇症型溶連菌に要注意、厚労省 昨年941人で過去最多

-
コロナ感染者、9週連続増 1医療機関当たり10人超に

-
PFAS許容量、従来通り 人の摂取、食品安全委

-
医療機関半数以上で不具合、大分 マイナ保険証、調査結果を公表

-
正常な月経とは? 静岡の専門学校で講義、浜松医大特任准教授

-
静岡県内22施設で学級・学年閉鎖 インフルエンザ

-
小児がん10年生存70~90% 初集計、大人より高率

-
不妊治療支援で初の条例化、兵庫 先進医療費を補助

-
DMATの活動期間「短い」 石川・珠洲市で救急対応の医師指摘 1泊2日のみの隊も、搬送時間もネックに

-
静岡県内28施設で学級・学年閉鎖 インフルエンザ

-
若者の市販薬乱用 背景には社会的孤立(竹下秀司/静岡県病院薬剤師会理事)【もっと広がる クスリの世界】

-
静岡県内6施設で学級、学年閉鎖閉鎖 インフルエンザ

-
新型コロナ、2週連続患者4割増「第10波に」 静岡県、感染拡大で注意報

-
静岡県内10施設で学級閉鎖 インフルエンザ

-
マイナ保険証利用、4・29% 8カ月連続低下、促進策を検討

-
小児がん患者に適応外薬 早期承認向け臨床研究開始

-
新型コロナ、8週連続で増加 厚労省「定期的な換気を」

-
静岡県内13施設で学年、学級閉鎖 インフルエンザ

-
歯周病検診に20歳、30歳追加 4月以降、若年患者増加で厚労省

-
静岡県の花粉飛散 1月下旬から 気象会社予想

-
被災者は医療介護、自己負担免除 年金保険料も、厚労省が支援策

-
花粉飛散、1月下旬からと予想 暖冬の影響、平年より早く

-
南伊豆の中学校で学年閉鎖 新型コロナ

-
富士中央病院 現地建て替え 市長方針 開院31年度に前倒し

-
かかりつけ歯科 どう選ぶ? まず健診で雰囲気確かめて(露木良治/静岡県歯科医師会生涯研修部)【歯の診察室】

-
静岡県内3小学校で学級・学年閉鎖 インフルエンザ

-
若い世代に「献血協力を」 2月までキャンペーン

-
コロナ医療費、4月から負担増 国内初確認4年、「第10波」も

-
中国、コロナの感染拡大を予想 新変異株が主流と見通し

-
移動薬局車が石川へ 静岡県薬剤師会 医薬品不足受け避難所で調剤

-
赤ちゃん寝かせる環境整えたい 窒息事故を防ぐ対策大切(静岡県こども家庭課)【親子の相談室】

-
浜松医大病院、血液がん治療で実績 CAR―T細胞療法、難治性患者も効果

-
静岡県内医療従事者 看護師ら能登半島被災地へ次々

-
コロナ感染、静岡県内注意報目前 インフルは急減

-
コロナ患者急増、インフルは減 静岡県感染症週報(1月1~7日)

-
若年性認知症 考えよう 2月4日、清水町で映画上映

-
心臓テーマに最新治療解説 浜松市中央区で13日講座

-
新型コロナ感染、7週連続増 石川は前週比1・56倍

-
インフルエンザ患者、4週連続減 前週比0・58倍、厚労省

-
カネミ患者へその緒調査へ 子や孫世代の救済目指す

-
患者17人個人情報 医師論文で漏えい 磐田市立総合病院

-
避難生活で命と健康守るには? 水分不足、体の冷えに注意 予防につま先立ち運動も【能登地震】

-
静岡県内2施設で学級閉鎖 インフルエンザ

-
珠洲市の病院「毎日がヤマ場」 浜松・聖隷三方原病院の派遣医師 発災124時間後救出の女性にも対応

-
ゲノム編集治療、承認広がる 重い貧血にノーベル化学賞の技術

-
インフルエンザ患者、微減 新型コロナは1・27倍 静岡県感染症週報(12月25~31日)

-
静岡県内1施設で学級閉鎖 インフルエンザ

-
治療に伴う外見変化に特化 相談窓口を開設 静岡がんセンター

-
新型コロナ、6週連続で増加 年末分、被災地で拡大懸念

-
インフル患者、3週連続減 昨年末、前週比0・94倍

-
救急搬送にマイナ保険証活用 迅速化へ47消防本部で試験運用

-
静岡県内の医療・福祉職 石川県被災各地の要配慮者支援へ派遣相次ぐ 「寄り添った活動を」

-
長期化する断水、感染症流行に危機感あらわ 能登地震、磐田市立総合病院DMATが報告

-
ノロウイルスなど30人報告 「避難所の衛生対策重要」

-
在宅医療の質向上へ 監視システムで急変“予知” 磐田の安間院長、開発進める

-
腸活、何をすれば 「善玉菌」意識し、食事見直し【知って、いかす 健康食品①】

-
インフル患者、2週連続減 昨年12月、前週比0・77倍

-
新型コロナ感染、5週連続増 昨年12月、前週比1・10倍

-
医療に影響、透析停止も 職員「野戦病院のよう」

-
認知症基本法、新年に施行 本人、家族の意見反映

-
インフル減少も警報継続、コロナは微増 静岡県感染症週報(12月18~24日)

-
静岡県内2施設で学年・全園閉鎖 インフルエンザ

-
中国や米国でコロナ変異株 「JN・1」感染拡大

-
ロボット手術「過失なし」 長崎大病院、術後死亡で調査

-
コロナワクチン4人誤接種 山口、インフルと取り違え

-
国民に良い薬届け、競争力戻す 政府の創薬向上会議が初開催

-
マイナ保険証利用4・33% 11月、7カ月連続低下

-
後発品不正相次ぎ 医薬品製造の監視強化 静岡県、品質確保へ全施設に無通告査察

-
静岡県内4施設で学級閉鎖 インフルエンザ

-
骨粗しょう症 服薬間隔 長いもの多く【もっと広がる クスリの世界】

-
認知症薬「レカネマブ」投与開始 東京のセンター、50代女性に

-
血液製剤不足、治療に支障 厚労省が安定供給へ輸入計画変更

-
インフル患者数減も警報継続 コロナはやや増 静岡県感染症週報(12月11~17日)

-
デング熱、23年に発生急増 5千人死亡、WHO

-
鼻粘膜抗体がウイルス排出抑制? コロナ感染拡大防止も、名古屋大

-
神戸徳洲会病院で70代患者死亡 糖尿病の既往歴見落としか

-
インフル患者数、定点0・89倍 前週比減も23道県で警報級

-
コロナ感染者、4週連続で増加 前週比1・18倍

-
介護職員の高齢者虐待が最多更新 22年度856件、国調査

-
静岡県内10施設で学級・学年閉鎖 インフルエンザ

-
コロナ定期接種 7000円に 来年度、高齢者ら自己負担

-
イヌの尿からiPS細胞効率作製 将来の治療応用に期待

-
コロナ定期接種、7千円に 来年度、高齢者ら自己負担

-
健康保険証、24年12月廃止へ マイナ一本化、最長1年の猶予

-
小児がん、臨床研究を了承 未承認薬の投与、厚労省会議

-
成人は睡眠6時間以上を推奨 健康づくりで厚労省ガイド

-
iPSで子宮頸がん縮小に成功 来夏に治験開始、順天堂大

-
静岡県内46施設で学級・学年閉鎖 インフルエンザ

-
AIが化学実験を立案、実行も 米カーネギーメロン大が開発

-
コロナ、ワクチン国際枠組み終了 年末で平常対応に

-
妊婦拒否巡り適切対応要請 提供精子利用、国が文書

-
社会保障費伸び圧縮、3報酬改定 1500億円、診療は全体で減

-
5種混合ワクチン、来年4月から 乳幼児の定期接種で

-
介護施設の相部屋、月8千円負担 25年度中に開始、厚労省

-
感染症危機に備え三つの目標 行動計画改定へ専門家意見

-
ハイブリッドERなど最新設備導入 浜松医療センター 新棟完成

-
病気と闘う子どもに笑顔と勇気を ディズニー、静岡県立こども病院に“魔法”の壁紙

-
指しゃぶりで歯並び心配 マウスピース型装置で改善も【歯の診察室】

-
短時間の大量飲酒に注意 年末年始、厚労省呼びかけ

-
市販薬、20歳未満に乱用対策 多量購入禁止へ制度見直し





 いい茶
いい茶





























































































































































































































































































































































































